医薬安全性 重点テーマと取り組み
重点テーマ
以下の3つを戦略の重点テーマとして、医薬安全性向上に向けた取り組みを進めています。
1. 非臨床・臨床データから副作用機序を解明し安全対策に活かす
ロシュ社やアカデミアなどのパートナーと協力し、リアルワールドデータやバイオマーカーを活用し、患者層別の安全性プロファイルを解析します。さらに、遺伝子情報、併存疾患などの患者背景因子と安全性の関連を科学的に解明し、個々の患者さんに最適な治療選択を支援するエビデンスを創出します。
2. 予見性と重症化予防を目指し、市販後早期に安全性データを創出する
開発早期から潜在的な安全性リスクを予測・評価し、包括的なリスク管理計画を策定しています。不足しているデータを特定し、副作用の予見・重篤化の予防につなげています。市販後早期にデータを創出することで、患者さんがより安全に治療をうけられるようにします。
3. 適正使用を推進し、患者さん・医療関係者に安全安心を届ける
製品の安全性情報を、国内外から迅速かつ網羅的に収集・分析し、継続的なモニタリングを通じて、製品の安全性プロファイルを常に最新の状態に保ちます。
それらの情報を、デジタル技術、臨床現場・患者さんのニーズと組み合わせ、最適な安全対策として提供することで、医療現場での製品の適正使用を推進します。
具体的な取り組み
3つの重点テーマに基づいた、具体的な取り組みをご紹介します。
1. 安全性情報の収集・管理、リスクアセスメント
治験では得られない実際の診療下での安全性情報を、医療機関からの報告や文献・学会情報を介して収集するとともに、全例調査やデータベース調査を含む製造販売後調査により能動的に収集しています。また、医療機関から収集した安全性情報を、疫学を含む多⾓的な⼿法でリスクアセスメントを実施しています。安全性プロファイルを継続的に検討することで、市販後の医薬品安全性監視活動を推進しています。得られた結果は医療機関に情報提供するとともに、学会や論文などで公表しています。これに加え、多くの抗がん剤や革新的なバイオ医薬品などでは、流通管理や使用状況の確認など、さらに広範囲かつ厳格な管理手法を導入し、安全性評価やその対策に活かしています。
2. 対処型の安全対策から予測予防型の安全対策への転換
従来の市販後医薬品安全性監視活動は、医療機関から収集した情報をもとにリスクアセスメントや安全性プロファイルの検討を行う「対処型」が中心でした。現在はこれに加え、事前に様々な知見を踏まえて仮説を立て、検証することで、承認後の個々の患者さんのリスクを予測し、副作用の発生および重篤化などを回避する取り組みを強化しています。
この「予防型」の市販後安全性監視活動を通じて、市販直後から患者さんが安心して治療に専念できる状態を目指します。
3. 安全性コミュニケーション
患者団体と協働し、実臨床において「患者さんが知りたい情報」や「患者さんに知っておいて欲しい情報」を、資材をはじめとした様々なソリューションとして提供しています。
患者さんの特性に応じ迅速な情報提供をするため、「調査・副作用データベース(DB)ツール」を2016年より運用しています。システムを刷新し、現在は医療関係者向けウェブサイト上で、医療関係者が必要な時に当社の製品に関する副作用情報にアクセスいただくことが可能となりました。直感的に操作いただけるよう、ユーザーインターフェースの改良なども行っています。こうした情報提供基盤の継続的な改善により、患者さん一人ひとりに合わせた安全性情報をよりスムーズにお届け出来るよう努めています。
中外製薬における安全性情報の収集・蓄積分析・提供サイクル
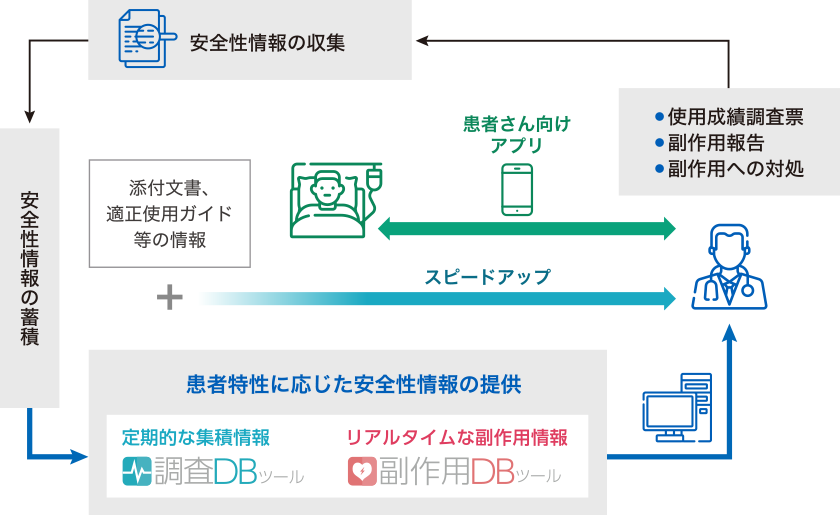
中外製薬では、患者さんと医療関係者とのコミュニケーションを円滑にし、患者さんにより安心して治療を受けていただくための取り組みを継続的に強化しています。