「制御性T細胞」をつくる・増やす-中外製薬と大阪大学免疫学フロンティア研究センターの共同研究チームが挑む細胞療法の可能性
- イノベーション
- 研究開発

制御性T細胞(Treg)とは何か?
私たちの体には、外敵から身を守る複雑な免疫システムが備わっています。このシステムの中で、制御性T細胞(Regulatory T cells、略してTreg)は非常に重要な役割を果たしています。Tregは体内の免疫細胞(リンパ球など)のわずか数%を占めるに過ぎませんが、自己に対する免疫反応を抑制する働きがあります。Tregの存在は1995年に坂口志文先生が提唱し、その機能が次第に明らかになりました*2。
Tregの主な役割は、他の免疫細胞の活動を調整することです。例えば、体内で過剰な免疫反応が起きそうになった時、Tregはそれを抑制します。しかし、Tregの機能が低下すると、免疫システムのバランスが崩れ、IPEX症候群をはじめとして関節リウマチや1型糖尿病、多発性硬化症などの自己免疫疾患を引き起こす可能性があります。一方で、Tregが過剰に働くと、がん細胞に対する免疫反応を抑制してしまい、がんの増悪につながる可能性があります*3。
このように免疫に広く関わるTregを増やしたり、除去したりすることで、病気を治療しようという研究が世界で進められています。
IPEX症候群とは:FOXP3遺伝子の異常が原因で免疫異常を呈する症候群で、IPEXはimmune dysregulation、polyendocrinopathy、enteropathy、X-linkedの頭文字。重症のアレルギー、自己免疫性の甲状腺異常やⅠ型糖尿病、炎症性腸疾患を呈する*4
FoxP3発現制御ネットワークの解明から、誘導型制御性T細胞(iTreg)細胞療法の可能性へ
今回、大阪大学IFReCと中外製薬の共同研究チームはTreg制御の新たなしくみを発見し、さらに、そのしくみをコントロールして自己免疫疾患を治療する可能性を見いだしました(Nature. 2025 Mar 26)。鍵となるのは、FoxP3というTregの分化と機能に不可欠なタンパク質で、Tregのマスターレギュレーターとして知られています。
「まず、ゲノムワイドCRISPR KOスクリーニングを用い約2万のヒト遺伝子の中でFoxP3誘導・発現制御に関与するものを網羅的に調べ、重要な因子を数百個に絞りこみました。次にシングルセル解析で個々の因子のノックアウト(目的の遺伝子の働きを抑えること)による遺伝子発現変化とFoxP3タンパク質発現変化の関係性からFoxP3制御シグナル経路とその関連因子群を明らかにしました。ゲノムワイドCRISPR KOスクリーニングとシングルセル解析を組み合わせることで、FoxP3発現抑制ネットワークの中心としてRBPJというタンパク質を同定できたのが、大きな発見でした」と中外製薬の研究員である木林達也は語ります。
CRISPR KOスクリーニングとは:CRISPR-Cas9とよばれるゲノム編集技術を用いて、特定の機能をもつ遺伝子を包括的に検出する手法。特定の遺伝子の機能を失わせて、その従来の役割を研究する「遺伝子ノックアウト」をゲノムスケールで行う
シングルセル解析とは:細胞のはたらきを解析する手法で、個々の細胞ごとにタンパク質やmRNAの発現データを取得・分析する。バルクセル解析が複数細胞の平均データを得るのに対し、シングルセル解析では個体内の細胞の多様性をより詳細に捉えることができる。今回の阪大-中外の研究論文でのシングルセル解析では、細胞の固定・膜透過の方法を工夫し技術的に難しかった細胞内のタンパク質とmRNAの同時検出・解析を可能とした。また、遺伝子編集された個々の細胞を同定する技術(Perturb-seq)も取り入れ、解析の解像度向上とスループットを両立させた
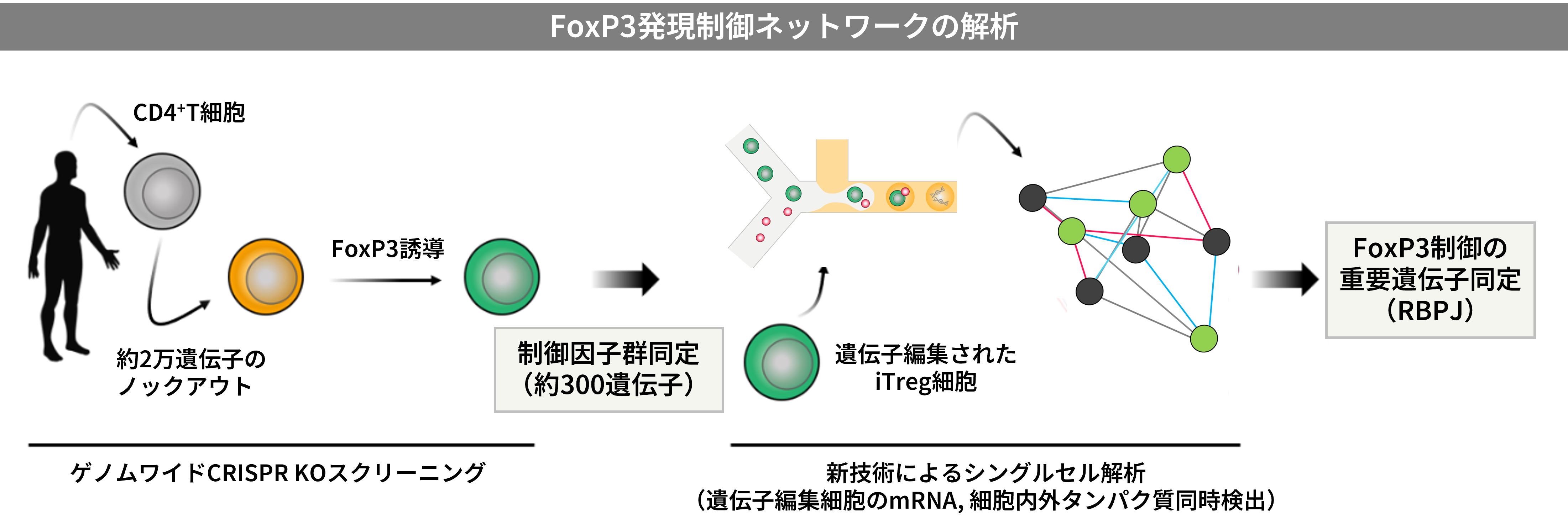
このようにTregにおけるFoxP3の発現制御ネットワークを明らかにした後、共同研究チームは「Treg細胞療法」の可能性を検証しました。
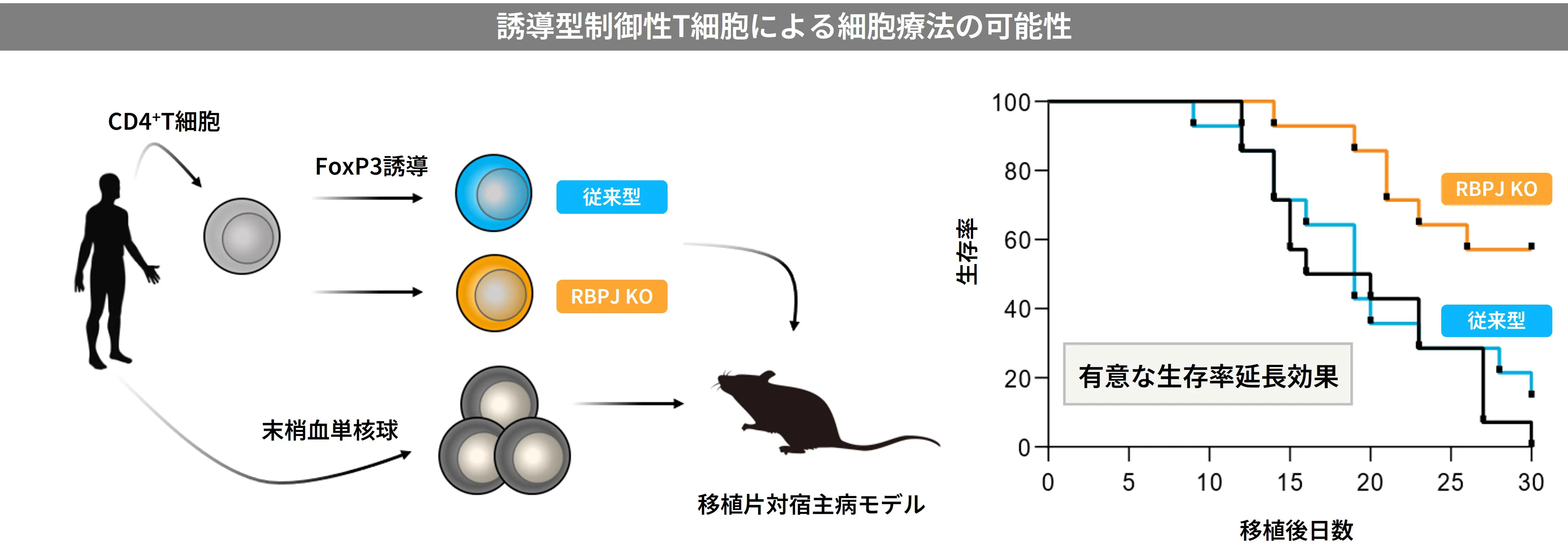
Treg細胞療法は、がん領域での免疫チェックポイント阻害剤やCAR-T細胞療法と並び、自己免疫疾患領域で注目される免疫治療のアプローチです。患者さん由来の制御性T細胞を生体外で増殖させ、体内に戻して免疫機能のバランスを正常化させます。近年開発が加速するCAR-Treg療法は病態に関連する1つ(または少数) の自己抗原を標的とするのに対し、誘導型Treg(in vitro induced Treg、略してiTreg)療法は関連する自己抗原群全体を標的にするのが特徴です。
「動物実験で、RBPJをノックアウトしたヒト末梢血由来のT細胞から誘導した制御性T細胞(RBPJ KO-iTreg)を動物に移入しました。すると、iTreg細胞療法は、生存率に悪影響を及ぼす拒絶免疫反応をより強く抑制することが確認できたのです。今回の研究成果は、iTregの誘導効率や機能・安定性の向上につながる重要な知見を見出したと言えるでしょう(木林)」。
免疫チェックポイント阻害剤とは: がん細胞が免疫細胞の攻撃を逃れる仕組みを解除して、免疫細胞の力を回復させる薬剤
CAR-T細胞療法とは:患者さん自身の血液からT細胞を取り出し、特定のがん抗原を認識させる遺伝子改変により、がん細胞を攻撃する治療法
産学連携がもたらす研究の進展、オープンイノベーションに向けて
中外製薬は、独自の創薬技術やノウハウと、アカデミアでの新しい発見を互いに提供して免疫学に関する先端的研究の成果の社会還元を目指す取組みとして、大阪大学との包括連携契約のもとで2017年より大阪大学免疫学フロンティア研究センター(IFReC)と先端的な免疫学研究活動に関わるさまざまな共同研究プロジェクトを進めています。
木林は、「制御性T細胞における科学的な意義と治療への応用の両方をつなぐ研究ができました」と話します。
「私は薬理研究を専門とし、中外の研究所から8年前にIFReCの連携推進ラボに派遣されました。今回Natureに掲載された研究論文のテーマは、坂口先生はじめIFReCの先生方とゼロから議論してスタートしたものです。信頼関係を築くことが、オープンイノベーションを進める上で最も重要だと思います。そして、研究の成果がiTreg細胞療法の実用化につながり、患者さんに届けられるには、まだ何年も時間がかかると思います。しかし、その実現に向けた大きな一歩となったと思います(木林)」。

共同研究者である坂口志文先生は、「Tregを減らしてがん治療に、あるいはTregをうまく増やして自己免疫疾患の治療に応用できないか?という研究の世界の潮流の中で、木林さんは非常に良い仕事をしてくれました。」と今回の発見を評価します。「情報なら誰でも手に入る今、大事なのは“研究は人がやるもの”ということ。新しい技術や知識を習得したら研究が進むわけではありません。アカデミアと企業が一緒に研究することで刺激し合い、一人ではできない新しいアイデアが生まれます。企業の研究者がIFReCで基礎研究に携わり、経験を企業に持ち帰ることは人材育成につながるでしょう。長い目で、日本の製薬企業の研究力の強化に貢献していきたい。」とオープンイノベーションに向けた想いを述べました。
画期的な医薬品の創出に向け、オープンイノベーションを加速する中外製薬。産学連携による研究のさらなる発展に、今後も注目が集まります。
参考文献
*1 Chen, K.Y., Kibayashi, T. et al.:Genome-wide CRISPR screen in human T cells reveals regulators of FOXP3. Nature (2025). doi: 10.1038/s41586-025-08795-5.
*2 Sakaguchi, S., et al.:Immunologic self-tolerance maintained by activated T cells expressing IL-2 receptor alpha-chains (CD25). Breakdown of a single mechanism of self-tolerance causes various autoimmune diseases. J Immunol., 155(3), 1151-64 (1995)
*3 Wadell, C.M. et al.:Harnessing the biology of regulatory T cells to treat disease. Nat Rev Drug Discov., 24(2), 93-111 (2025)
*4 Bacchetta, R., Roncarolo, M.G.:IPEX syndrome from diagnosis to cure, learning along the way. J Allergy Clin Immunol., 153(3), 595-605 (2024)
【関連情報】
https://www.chugai-pharm.co.jp/profile/rd/features.html#sec02
木林達也(創薬薬理第二研究部)
2013年中外製薬入社。専門は薬理学。入社4年目までに主にがん領域の抗体医薬品候補の薬効評価、新規標的探索、新規抗体技術開発などに従事。旧鎌倉研究所、旧富士御殿場研究所を経て、2017年4月に大阪大学免疫学フロンティア研究センターに派遣され、実験免疫学 坂口志文教授のもとで制御性T細胞に関わる共同研究に取り組む。

記載内容・所属は2025年3月時点のものです。


