


がん治療は「個別化」の時代へ
広がる治療の可能性
日本人の死因第1位であり、いまや国民の2人に1人がかかる病気である「がん」は、遺伝子の変異によって起こる病気だ。
いま 「がんゲノム医療」が、治療の可能性を広げるとして注目されている。
がんが発生した臓器ごとに治療法を考えるのではなく、一人ひとりの遺伝子の変異を解析することで最適な治療法を提供するというものだ。
がんゲノム医療とはどのようなものなのか、何が期待できるのかに迫る。

そもそも「がんゲノム医療」とは
従来のがん治療では「体のどこにがんができたのか?」に注目し、臓器ごとに一律の治療を行ってきた。
一方、「がんゲノム医療」は、がんの原因である遺伝子の変異を解析。臓器ごとではなく、個人の遺伝子の変異に合わせた”オーダーメード”な治療を選択できる可能性が広がるのが特長だ。
がんは、遺伝子に生じた変異が原因で起こる病気だ。
人の体をかたちづくるもとである細胞が何らかの原因で遺伝子変異を起こし、それが修復されないと、がん化して際限なく増殖してしまうことがある。増殖した細胞はやがて周囲の正常な組織や臓器に広がり、臓器不全を起こすことで患者を衰弱させてしまう。
がんは日本人の死因第1位であり、多くの人がかかる可能性がある病気だ。
日本人が一生のうちに
がんと診断される確率※1
男性
44.6%
2人に1人
女性
31.4%
2人に1人
日本人ががんで死亡する確率※2
男性
7.6%
4人に1人
女性
0.0%
6人に1人
※1:2020年のデータに基づく ※2:2022年のデータに基づく
出典:国立研究開発法人国立がん研究センター「最新がん統計のまとめ」
がん治療は、主に臓器ごとに治療が行われている。例えば、肺、胃、大腸、乳がんなどの分類で、それぞれの臓器に特化した治療法が開発されてきた。
近年進展してきたのが「がんゲノム医療」だ。がんの原因となる遺伝子の変異を特定し、それに基づいて適した治療法が選択できる可能性があると期待され、注目を集めている。
これまでは、がんが生じた臓器ごとに定められた治療薬を使う方針が主だった
がんゲノム医療では、がんが発生した臓器だけでなく、一人ひとりの遺伝子変異に基づいて適した治療薬を選べる可能性がある
がん治療の歴史を紐解く
手術や放射線照射などの局所的な治療法に加え、全身に対して行える薬物療法が登場。がんの治療法が広がっていった。
がんの治療には、がん細胞の塊を物理的に切り取る「手術療法」や、高いエネルギーを持つ光を当てることでがん細胞を壊す「放射線療法」が存在していた。しかし、いずれもがんが発症している場所に対して局所的に行う治療だった。
そこに1940年代、「抗がん剤」が登場する。
抗がん剤の始まりは、20世紀初めに使われた化学兵器「マスタードガス」。人が曝露すると、白血球の減少が見られることが発見されたのだ。毒性により、白血球の分裂・増殖が抑えられたためだった。
がんは悪性細胞が際限なく増殖してしまう病気だ。マスタードガスの特徴を応用すれば、がん細胞の分裂増殖を抑えられるのではないか――。
この発見を契機に、抗がん剤創薬の歴史がスタート。がん細胞の分裂・増殖を阻害するアプローチが異なる様々な抗がん剤が登場した。
しかし従来の抗がん剤は増殖が速い細胞の分裂を抑え、
死滅させるというものだった。
そのため、がん細胞だけでなく正常な細胞も攻撃してしまい、
嘔吐や脱毛などの副作用が患者の大きな負担となるのが課題だった。
がん細胞を、ピンポイントで攻撃する方法はないのか。
模索が続けられた。
がん発生メカニズム解明により開かれた治療薬の進歩
研究により、がんが遺伝子の変異で起こる病気であることが明らかに。
単にがん細胞を切除/破壊するのではなく、がんの遺伝子変化により作られる分子(タンパク質)に働きかけて増殖を防いだり、免疫細胞ががん細胞を攻撃する力を保ったりという、新しいアプローチの治療薬が登場してきた。
がん治療に大きなイノベーションが生まれたのは、がんが遺伝子の変異によって起こる病気だということが分かってきたからだ。
それまでがん発生のメカニズムは全く分かっていなかった。しかし1980年代に人のがん発生に関わる遺伝子が発見されたことで、研究は新たなフェーズに入る。
がん細胞に特徴的な遺伝子変異や、それによって活性化される異常なタンパク質を特定することで、がんの発生に関わるさまざまな分子の働きが次々と解明されていったのだ。
これらの発見を基に、新しい種類の薬の開発が始まった。
がん細胞だけでなく正常な細胞にも攻撃的に作用してしまう従来の薬と異なり、新しい種類の薬は、がんに関わる特定の分子(主にタンパク質)を狙って攻撃するように設計された。これが「分子標的薬」だ。
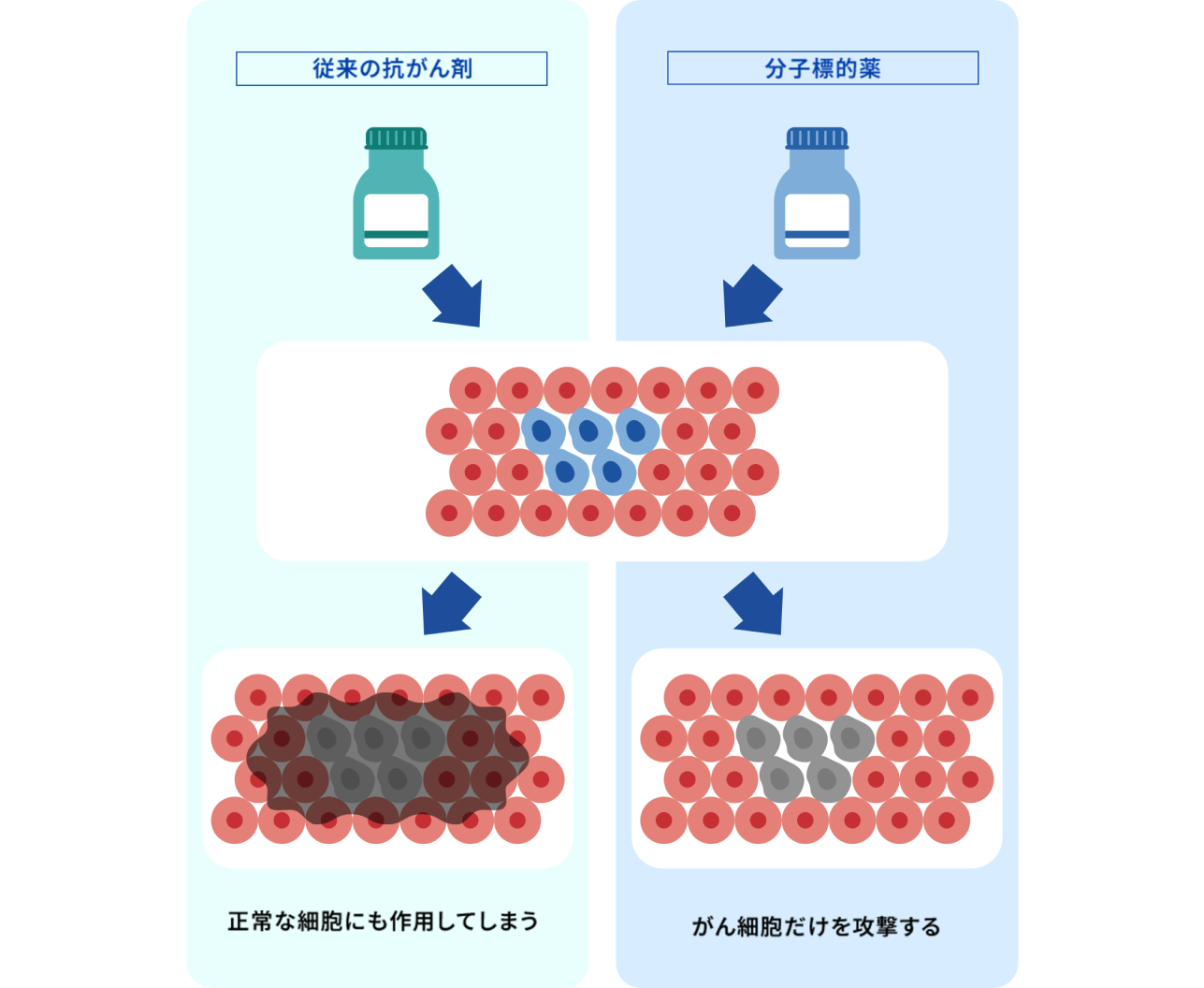
分子標的薬は、がん細胞の増殖や生存に重要な特定分子や経路を標的とし、その働きを阻害することでがんの成長を抑える。最初の分子標的薬が承認されたのは、2001年のことだった。
分子標的薬の登場により、多様なモダリティ(創薬技術の分類)における抗がん剤の開発はさらに進展。現在、分子標的薬には以下のようなタイプが存在している。
低分子医薬品
分子標的薬の中でも、分子量が小さな化合物。がん細胞を増殖させるタンパク質を標的に細胞内に入りこみ結合し、増殖を促す細胞内のシグナルを攻撃するように設計されている。
抗体医薬品
がん細胞などの細胞表面の目印となる抗原をピンポイントで狙い撃ちする薬で、高い治療効果と副作用の軽減が期待される。2014年に日本で初めて承認された「免疫チェックポイント阻害剤」は、がん細胞が免疫細胞の攻撃を逃れるしくみを解除し、免疫細胞ががん細胞を攻撃する力を保つ。
これらの創薬イノベーションにより、患者の治療満足度は以前よりも大きく向上している。
例えば肺がんでは、分子標的薬が登場した2000年代前半以降、治療満足度※や薬剤貢献度※が増加。1994年度から2019年度までの25年間で、治療満足度は11%から52%へ、薬剤貢献度は7%から83%へ伸びている。
新しい薬の開発が、がん治療を変えていっている。




出典:医薬産業政策研究所「アンメット・メディカル・ニーズに対する医薬品の開発・承認状況-2022年の動向-」および公益財団法人 ヒューマンサイエンス振興財団 国内基盤技術に関する調査報告書「60疾患に関する医療ニーズ調査」1994年度、2000年度、2005年度、2010年度、2014年度、2019年度をもとに中外製薬が作成
※「治療満足度」「薬剤貢献度」とは:ヒューマンサイエンス振興財団が1994年度から2019年度までの間、ほぼ5年に一度、一般内科医を対象に実施した調査によるもの。疾患ごとに、治療満足度は4つの選択肢(十分に満足/ある程度満足/不満足/治療が行えているとはいえない)のうち「十分に満足」あるいは「ある程度満足」と回答した医師の割合。薬剤貢献度は4つの選択肢(十分に貢献/ある程度貢献/あまり貢献していない/効く薬がない)のうち「十分に貢献」あるいは「ある程度貢献」と回答した医師の割合
国内で承認されている
主要ながん分子標的薬の数※1
2001年
0
2022年
0
国内で承認されている
免疫チェックポイント阻害剤の数※2
2014年
0
2024年
0
※1 出典:日本がん分子標的治療学会「JAMTTC News Letter」No.26-1(2022年3月発行)長浜バイオ大学・バイオサイエンス学部 水上民生氏の報告をもとに中外製薬が整理
※2 出典:AnswerNews「『オプジーボ』承認から10年…免疫チェックポイント阻害薬、一大市場形成も薬価制度に翻弄」(2024年8月6日公開)
がん遺伝子パネル検査の登場
遺伝子の変異を解析することで、特定の治療薬に効果が見込めるかどうかをあらかじめ検査できるように。
検査技術の進歩により、多数の遺伝子を一度に検査できる「がん遺伝子パネル検査」も可能になった。
分子標的薬が標的とする、病気の原因となるタンパク質は、遺伝子の変異によって生じる。がんを引き起こす原因となる「がん関連遺伝子」は、現在までに数百程度見つかっている。がん細胞の中に、標的の対象となる遺伝子の変異があるかどうかを調べることで、該当の分子標的薬が使えるかどうか検討可能になる。
2010年代からは、特定の分子標的薬の効果や副作用を事前に調べる「コンパニオン診断」が導入。がん細胞の中に分子標的薬の標的となるタンパク質が発現しているかを、コンパニオン診断薬を使って検査するというものだ。
しかし、一つひとつの遺伝子を順番に調べる必要があるため、時間がかかっていた。
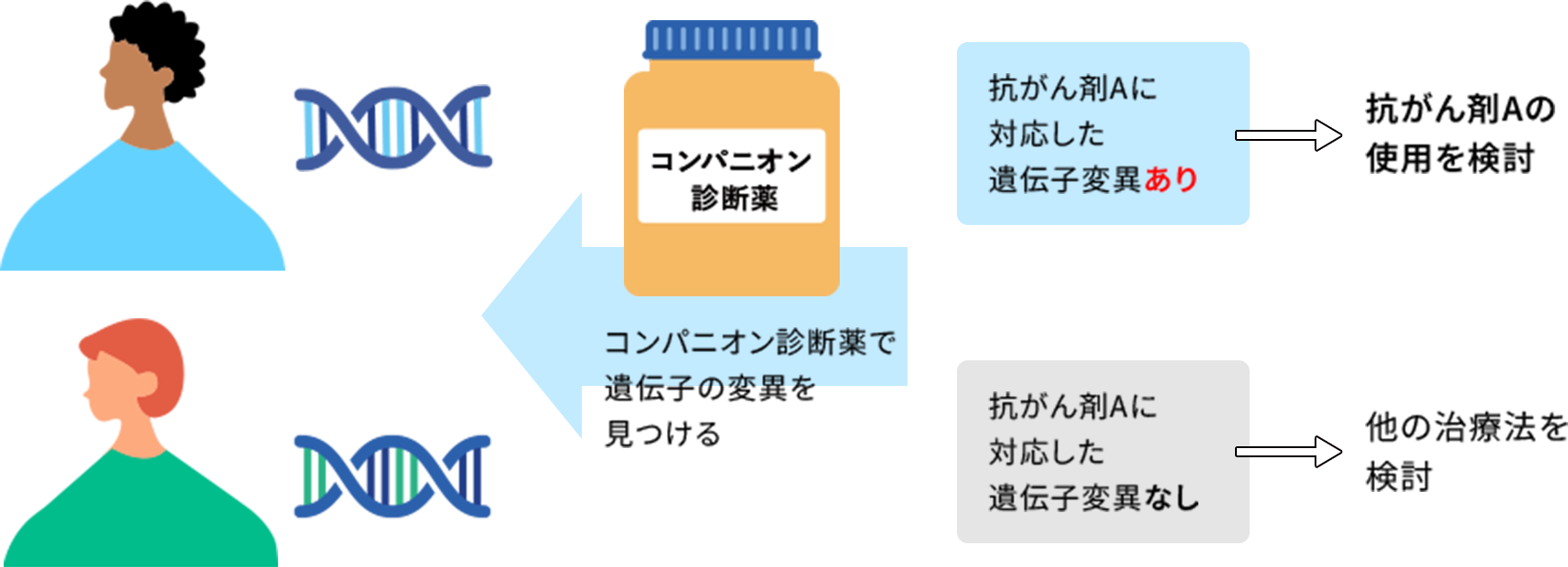
ゲノム医療の進展やデータ解析技術の飛躍的な進歩により、数十~数百程度の遺伝子を網羅的に検査できる「遺伝子パネル検査」が行えるようになった。特定の分子標的薬を使用するかどうかを判定するのではなく、複数の遺伝子を網羅的に検査できるため、結果を総合的に判断して最適な治療法を探すことができるのが特長だ。

2019年以降「次世代シークエンサー」という検査装置を用いた包括的がん関連遺伝子解析システムが登場し、がん種を横断的に診断できるようになった。
さらに、これまでの生検採取による検査だけでなく、血液採取による検査も可能になった。体への負担が少ないうえ、生体組織を検査する場合より遺伝子解析にかかる時間が短いため、がんの早期発見にも活用できると期待されている。
がん遺伝子パネル検査は現在、標準治療がない、または標準治療が終了(終了見込みも含む)となった固形がん患者を対象に保険適用の範囲となっている。
がんゲノム医療は、本格的な実用段階に入っているといえるだろう。
一方で、がん遺伝子パネル検査を受けても、
治療に結び付けられるのは現状9.4%に留まる。
- ・遺伝子に変異が見つからない
- ・薬剤を投与する基準に当てはまらない
- ・薬剤が日本で未承認
- ・治験・臨床試験の参加条件に合わない
- ・そもそも、治療薬が開発されていない
などが理由だ。

新薬創出にもつながる可能性があるがんゲノム医療
実際の治療に結び付けられる例はまだまだ少ないかも知れない。
しかし、がん遺伝子パネル検査で集められたデータは、がんの治療の可能性を広げることにも役立つ。
遺伝子パネル検査により集められたゲノム情報や診療情報は、国立研究開発法人 国立がん研究センターのがんゲノム情報管理センター(C-CAT)に、個人が特定されないかたちでプール。
がん遺伝子情報の変異を分析し、がんのしくみについて研究を進めたり、薬の効果や副作用といった情報を、臨床現場で役立てたりすることができる。分析したデータは、新しい治療薬の創出にも役立てられるのだ。
かつて不治の病だった肺結核は、治療薬の登場により治る病気になり、
かつて手術しか治療法のなかった胃潰瘍や十二指腸潰瘍は、薬で治せるようになった。
がんゲノム医療の進展により、より多くの患者に、最適な治療が提供できることが期待される。
そして、新たな薬を創り出すことができれば、がん治療の可能性はさらに拓かれていくはずだ。
国内におけるがん治療のリーディングカンパニーである中外製薬は、独自の技術とサイエンスで、がん遺伝子変異に対応した革新的な新薬やがんゲノム医療の両面からがん治療の進展に寄与し、患者の健康と幸せに貢献することを目指している。


