中外製薬にとってもnemolizumabは非常にユニークな存在です。アトピー性皮膚炎を対象とした、抗IL-31レセプターAヒト化モノクローナル抗体であり、中外製薬が初めて挑んだ皮膚科領域でのグローバル開発となります。
田中がnemolizumabのグローバルプロジェクトリーダーに就任したのは2008年9月。もともと研究所出身だった彼は、プロジェクトが立ち上がった当初から、IL-31そのものに強い興味を示していました。「とても面白いサイトカインで、主要な生理機能はかゆみを起こすこと。ほかの抗サイトカイン抗体のように免疫を抑制することもなさそうなので、安全に使える薬になるはず」と、直感的に感じたと言います。
プロジェクトのスタートとともに、メンバー全員が専門性を高めるため、皮膚科領域について学び始め、改めてアトピー性皮膚炎の重大さを再認識していきます。難治性の慢性疾患であり、長期間、有効な新薬が登場していない疾患。重度のそう痒は、眠れないなどの著しいQOLの低下を招き、かゆみとかきむしりの悪循環による皮膚病変は容姿も損ねてしまいます。特に小児や青年などの若い患者さんが多いことから、学習への妨げにもなるなど、患者さんとその家族にとって大きな負担となっていました。
「そこにはアンメットメディカルニーズがあり、新しい治療薬が渇望されていました。私たちにとっては未知の領域でしたが、皮膚科の先生方の意見を伺ううちに、これは成し遂げなければいけないチャレンジだと認識を深めていきました」と、田中。何もかも初めてであるならば、最初からグローバルスタディを視野に入れようと、異例の開発方針を打ち出します。
開発研究(詳細についてはP78をご参照ください)に移行するのとほぼ同時に、田中らは欧米の医師へアクセスを開始。早期プロジェクトでは当時は社内であまり例がない中、皮膚科領域の専門家からなるアドバイザリーボードを設置し、市場調査の範囲は国内だけでなく、グローバルに及びました。さらに、田中は、国内での第Ⅰ相臨床試験で患者さんも対象とすることを決定。がん以外の予定適応症の場合、これまでの臨床開発では第Ⅱ相から患者さんを含めるのが一般的であり、社内から疑問視する声もあがりました。
「新しい作用機序なので、もちろん前提として十分な安全性への配慮は大切ですが、かゆみに特化しているサイトカインのため、動物実験でも副作用が出現しなかったのです」と田中。当局への相談を社内で検討していたとき、薬事部のメンバーから「中外製薬として失うものはないのだから推し進めるべき」との強力な後押しもあり、nemolizumabのプロジェクトチーム全員が、この大いなるチャレンジに踏み出します。
「導出先としては、皮膚科領域を専門とする第三者企業への導出を想定していました」と田中は、画期的な新薬になり得るnemolizumabの開発が停滞しないよう、あらゆる方策を練っていました。そして、2011年9月に始まった第Ⅰ相臨床試験は、第Ⅱ相を先取りした形で実施。試験を3つのパートに分け、パートAでは日本人の健康成人、パートBでは白人の健康成人、パートCでは患者さんを組み入れ、1回の投与で薬効を確認しました。そこで良好な結果が得られ、それをもとに導出活動を開始しました。この手法はやがて中外製薬では一般的になり、第Ⅰ相臨床試験でearly PoCを取得するという新たな開発モデルの礎となったのです。
第Ⅱ相臨床試験の重要な目的は、用法・用量の設定です。将来、この新薬をグローバルで展開するのであれば、海外当局は欧米人での臨床成績を求めてくるのではと田中らは推測。さらに当時、日本の当局も国際共同治験への参加を推進し始めていたという背景もあり、中外製薬初となる単独による国際共同治験に踏み出します。
欧州では治験を実施する国ごとに届け出が必要で、かつ試験計画に各国特有の要求もありました。そのため田中らは、幾度も試験計画を修正することになり、試験期間は徐々に延びていきました。「すべてが初めてなので、あらゆることが課題でした。国や施設による違いは大きく、当時それを予測することは困難で、最終的に試験終了は予定より8カ月も遅延してしまいました」と、三極実施の難しさを田中は振り返ります。また、海外皮膚科領域で治験経験がない中外製薬は、現地の医師たちに認知されていないことも足かせとなりました。
しかし、その当時、皮膚科領域ではIL-31の阻害は新しい発見だったため、医師たちはやがて興味を示していき、第Ⅱ相国際共同治験を無事にスタートすることができました。パートAでの12週間の観察で主な薬効を確認し、パートBでは1年間の投与における有効性と安全性を確認。そのパートBも終了し、現在は論文掲載*7および学会発表*8が行われたところです。
第Ⅱ相国際共同治験の後、2016年7月にスイスのガルデルマ社と、2016年9月にマルホ株式会社(以下、マルホ社)と相次いでライセンス契約を締結し、nemolizumabは第三者企業への導出の道を歩み始めます。
ガルデルマ社は、皮膚科領域で高いプレゼンスを誇る世界的な製薬会社です。疾患や薬剤に対する思想も通じるところがありました。第Ⅱ相国際共同治験結果を目の当たりにした同社は、「これはファーストインクラスとなる、革新的な生物学的治療薬になるだろう」と評価し、契約へとつながりました。今後は、ガルデルマ社が日本および台湾を除く海外における臨床開発を推進し、中外製薬は治験薬の製造と提供を担っていきます。
そして、マルホ社は国内の皮膚科領域で卓越した経験と実績を有します。同社も早くからnemolizumabに高い関心を示していて、早期に新薬を患者さんに届けたいという思惑が一致したことから契約に至りました。
nemolizumabは、2015年8月より、透析そう痒症を対象とした第Ⅱ相臨床試験を国内で開始。透析そう痒症における国内開発および販売は、中外製薬が継続して実施していく予定です。
また、同プロジェクトは、中外製薬にとって初となる試みの連続だったという大きな特徴があります。背景に、当時の各本部の担当者からなるプロジェクトチームメンバーの強い熱意と決断力があったからだと田中は述懐。そして、あらゆる場面がターニングポイントではありましたが、そのたびに会社の全面的な支援によって乗り越えてこられたと言います。
「nemolizumabをはじめ、『SA237』やエミシズマブ(『ACE910』)、『アレセンサ』など、近年のこれらプロジェクトは、中外製薬をグローバルトップ製薬企業へ向かう道を拓いていったと思います。nemolizumabは第三者企業への導出も決まるなど、非常に幸運でしたが、会社全体が新しい方向へ進むきっかけであり、組織変革にもつながったことは喜ばしいことです。そんな最初のプロジェクトに携われたことに、私たちプロジェクトチーム全員は誇りに思っています」と語気を強めた田中。「私は、なんでも“初”というのが好きなんですよ」と屈託のない笑顔を見せながら、患者さんのための革新を続けることを約束していました。
皮膚疾患とnemolizumab
アトピー性皮膚炎は、表皮のバリア機能障害と抗原物質に対する過敏反応という2種類の機能異常に起因する多因子性疾患で、慢性に経過し、かゆみを伴う炎症性皮膚炎です。また、透析そう痒症は炎症を伴わない全身性の強いかゆみを引き起こし、アトピー性皮膚炎と同様に、患者さんのQOLを著しく低下させる原因となっています。
新薬の標的候補となる、さまざまな新分子の探索に取り組む中外分子医学研究所は、1999年にIL-31受容体を世界で初めてクローニングに成功しました。その当時はまだ生理機能が不明でしたが、2004年にIL-31がそう痒を引き起こすサイトカインであることが解明されました。中外製薬では、独自の抗体改変技術ACT-Ig*6を駆使してnemolizumabを創製。IL-31とその受容体の結合を競合的に阻害することによりIL-31の作用を抑制するnemolizumabは、革新的な新薬として全世界から期待されています。
- *6
- 抗体の半減期を延長する技術。抗体を負電荷に改変し、負電荷を有する血管内皮の細胞と反発させることにより、抗体の細胞内への取り込みを抑制
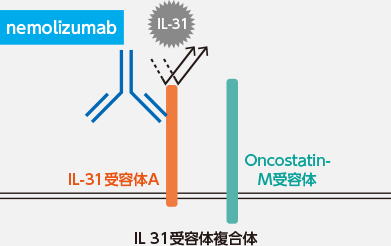
■ nemolizumab(抗IL-31受容体A抗体)- 作用機序
Galderma Pharma S.A. / Galderma S.A.
ガルデルマ社はスイス・ローザンヌに本社を置く、皮膚科に特化した製薬企業です。創業は1981年、現在、100カ国で製品を提供しており、皮膚科領域において幅広いポートフォリオを所有しています。世界の医療従事者と協力し、人々の生涯を通じた皮膚の健康ニーズを満たすべく、皮膚、髪、爪のためのエビデンスに基づいた、革新的なメディカルソリューションを提供する皮膚科領域のリーダーです。
マルホ株式会社
マルホ社は大阪市北区に本社を置く、医療用医薬品の研究・開発・製造・販売を行う製薬企業です。創業は1915年、従業員数は1,398名(2016年9月末時点)です。2016年9月期の売上高は700億744百万円でした。“Excellence in Dermatology”を長期ビジョンとして掲げ、皮膚科学領域での卓越した貢献を目指しています。