I B I 18の目標達成とトップ製薬企業像の実現、さらに将来にわたってグローバルでの成長を実現するためには、経営資源の選択と集中を加速し、グローバルでの競争力をさらに強化していく必要があります。トップ製薬企業の定量目標は堅調な進捗を見せていますが、先に申し上げたように、薬価制度をはじめとして、業界環境や競争環境はますます不透明さが増しています。
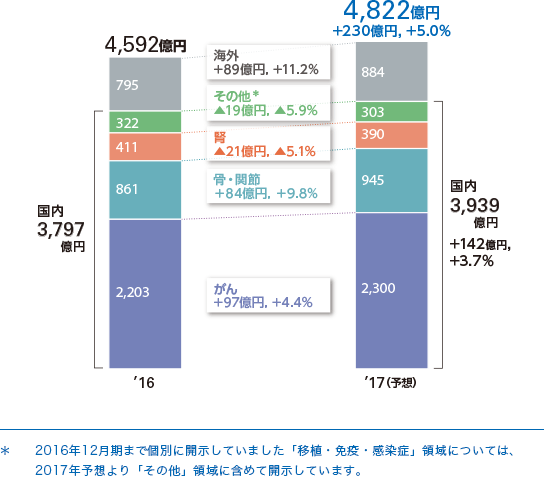
こうした中、中外製薬は、安定的な収入源としての「国内」と、自社創製品のグローバル展開による成長源としての「海外」を大きな2本柱として明確化し、それぞれの充実によって将来の成長に向けた強固な基盤づくりを推進していきます。
2017年は、「グローバル・国内成長ドライバーへの集中」「抗体改変プロジェクトの創出・中分子技術の開発」「ソリューション提供体制改革の実行」を重点テーマに掲げました。
成長ドライバーでは、引き続きエミシズマブ、アテゾリズマブ(「RG7446」)に経営資源を集中します。血友病Aを予定適応症としたエミシズマブでは、最速上市を目指して国内外で承認申請するとともに、グローバルでの需要拡大に対応すべく、生産体制の構築と浮間工場でのバイオ原薬製造設備の建設に着手しています。グローバルでの競争激化が見込まれるがん免疫療法アテゾリズマブでは、費用・人員を集中化させ、スピード競争に打ち勝っていきます。
創薬研究では、I B I 18の期間中に、独自技術を用いた改変抗体プロジェクトを2つ臨床開発段階に進めることを目指していきます。
中分子プロジェクトにおいても、いよいよ薬剤候補物質の創出が現実味を帯びており、非臨床初期プロジェクトの創出を目指し、ライブラリーの進化のほか、技術課題の解決を進めます。また基礎研究においても、2017年4月より包括連携パートナーであるIFReCの施設内に新しいラボを設置し、稼働させていきます。
ソリューション提供体制の改革については、グローバルでは各国の状況に合わせた効率的体制の構築が重要であり、海外子会社主導で改革をスピーディに推進します。また国内においては、医療制度の改革により2018年から都道府県主導の医療提供体制となることを前に、地域の実情にきめ細かに対応しながら、さらなる専門性を発揮すべく、営業・メディカル・安全性分野における組織改革を2017年4月に実行します(組織改革についての詳細は、P35「新たな国内ソリューション提供体制について」をご参照ください)。
2017年の業績は、国内外で「アレセンサ」をはじめとする新製品、主力製品が順調に成長することを見込み、売上収益5,205億円、Core営業利益920億円といずれも過去最高を予想しています。
2017年は申請ラッシュを迎えます。具体的には、国内外でのエミシズマブ(インヒビター保有対象)、海外の「アレセンサ」の1次治療、国内でのアテゾリズマブの2つの適応症の承認申請などを予定しています。また、2018年以降も多くの承認申請が控えています。
I B I 18で目指すのは、グローバルで飛躍し続ける企業への変革です。IBI 18の期間に申請を迎える多数の品目が売上に寄与するのはI B I 18以降ですが、これを飛躍的な成長フェーズとできるよう、事業活動のあらゆる分野で変革を進めていきます。エミシズマブ、アテゾリズマブ、nemolizumab、「SA237」といった患者さんに大きく貢献できる新薬候補品群、CPRからの創製品の連続創出、そして中分子品の創出など、将来の成長への道筋はすでに見えています。